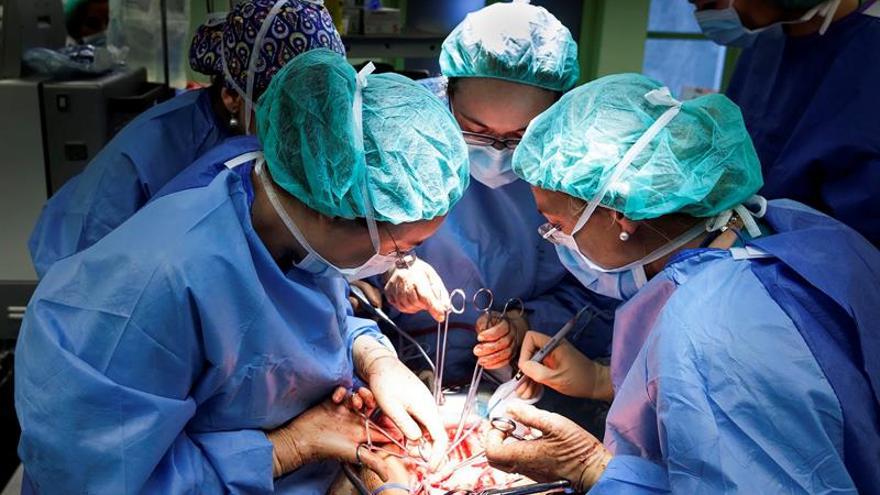
Human stem-cell-derived beta cells that have formed islet-like clusters in a mouse. Cells were transplanted to the kidney capsule and photographed 2 weeks later, by which time the beta cells were making insulin and had cured the diabetes in the mouse.
The Harvard Stem Cell Institute (HSCI), three of Harvard's clinical affiliates, and a biopharmaceutical company have formed an unusual collaboration to establish the Boston Autologous Islet Replacement Program (BAIRT) to accelerate a cure for diabetes.
Recent advancements in stem cell biology have provided an unprecedented opportunity to treat diabetes, researchers say. HSCI co-director Doug Melton has developed a process to generate virtually unlimited numbers of beta cells, which are insulin-producing cells in the pancreas, from stem cells in the lab. These stem-derived beta cells could be used to replace a person's beta cells to treat diabetes in the clinic.
The new program, designed by HSCI, Brigham and Women's Hospital (BWH), and the Joslin Diabetes Center (JDC), in collaboration with Semma Therapeutics (Semma) and the Dana-Farber Cancer Institute (DFCI), will work toward translating these stem cell discoveries into treatments that ultimately may help to cure diabetic patients.
Generating clinical-grade, pluripotent stem cells suitable for use in patients will take time. The first cell transplant conducted by BAIRT is projected to be at least three to four years away. The initial clinical trial will enroll a very small, very select group of patients: individuals who have had their pancreas surgically removed because they had intractable pancreatitis or similar conditions and who have not shown signs of islet autoimmunity (the body attacking its own insulin-producing cells). The initial trial will test both the safety of the stem cell-derived beta cells and make an initial assessment of their efficacy. The program is intended to leverage the stem cell and beta cell capabilities along with the clinical expertise and resources of the participating institutions to bring a novel therapy rapidly to patients.
During the first phase of the program, DFCI, HSCI, and Semma, of which Melton was the scientific founder, will work together to develop and optimize the stem cell derivation protocol. BWH and JDC will work together to screen, characterize, and identify suitable patients. In the next phase, the cell production facility at DFCI will derive stem cells from patients and manufacture the beta cell products using Semma's differentiation protocol. BWH will perform the transplants, and both BWH and JDC will follow the patients.
"No one institution anywhere has the expertise and technical abilities to make this kind of clinical trial possible," said Melton. "But in the unique Harvard biomedical ecosystem, we are able to bring all the necessary expertise and infrastructure to bear. I cannot begin to express the gratitude I feel to the leaders of Brigham and Women's, Joslin Diabetes Center, and Dana-Farber for the eagerness with which they have embraced this project."
Peter Amenta, president of Joslin, said, "One of our highest priorities at Joslin Diabetes Center has been to bring stem cell-based beta cell replacement therapy to people living with diabetes. We are excited to be working with other Boston leaders in academia and industry to make this a reality. Joslin has a long history of expertise in beta cell research, immunology, and novel diabetes clinical trials. This will synergize nicely with the complementary strengths of our partners. Combining our efforts is a clear and logical step."
The Brigham's involvement in the project grew out of its international reputation as a leader in transplantation research and surgery. "This project builds on our pioneering work in transplantation and exemplifies the Brigham's commitment to fostering discovery and innovation in order to translate research advancements into new therapies and treatments for our patients," said Betsy Nabel, president of Brigham and Women's Health Care. "We're excited to partner with these esteemed institutions to push the boundaries in improving the care and treatment of patients with diabetes."
While establishing the transplantation center and preparing the cells for the first trial might seem far from Dana-Farber's mission, in fact for almost 40 years the institute has been performing blood stem cell transplants, which the public better knows as bone marrow transplants. To prepare the cells for those procedures, DFCI established the only Good Manufacturing Practice (GMP) cell production program in Boston.
"The Connell O'Reilly Cell Manipulation Core Facility (CMCF) at Dana-Farber Cancer Institute has supported the bone marrow stem cell transplant programs for adults and children with our partners at Brigham and Women's Hospital and Boston Children's Hospital for more than 20 years," said Dana-Farber president and CEO Edward J. Benz Jr. "With a highly trained staff who have extensive experience in the processing of cells for individual patients, our CMCF has the unique ability to undertake complex cell-processing methods and manufacture cells to meet stringent FDA requirements. The ability to create insulin-secreting cells for individual patients is truly groundbreaking, and we are excited to be part of this innovative program."
Robert Millman, CEO of Semma Therapeutics, the company Melton founded to bring his cells to patients, said, "Semma is committed to advancing cell therapy for the treatment of diabetes. This relationship will provide Semma an additional opportunity to work with world-leading institutions in developing clinical applications of stem-cell-derived beta cells."
Explore further: Stem-cell research to help Europe's growing population of diabetics