«Conseguir regenerar el cartílago es digno de premio Nobel», dice, medio en serio medio en broma, Angelo Tapia, veterinario del equipo de investigación del Centro de Mínima Invasión Jesús Usón que trabaja en el proyecto Cartman.
Este proyecto tiene el objetivo de diseñar un biomaterial implantable en el cuerpo humano y que sea aplicable al tratamiento de las lesiones osteoarticulares. Esto es, lograr que las personas afectadas de osteoartritis, patología que daña el cartílago de las articulaciones, puedan mejorar de sus lesiones mediante un proceso de cirugía de mínima invasión.
Pero para llegar a conseguirlo es necesario el desarrollo de una investigación multidisciplinar en la que participan tres grupos. «El primero es una empresa, el segundo es el hospital de Bilbao y el tercero nosotros, en el Centro de Cirugía», manifiesta Javier García, investigador principal del equipo cacereño.
Cada una de las partes tiene su función. La de la empresa es desarrollar la máquina que fabrica el biomaterial y el grupo del hospital realiza los ensayos in vitro, para ver cómo se comportan las células humanas con el biomaterial. «Una vez que se pasa del ensayo in vitro llegan las pruebas en los modelos animales, que es lo que realizamos aquí aplicando el modelo porcino», expone García sobre lo que se denomina la fase preclínica del conjunto del proyecto, que a su vez está dividida en varios procesos.
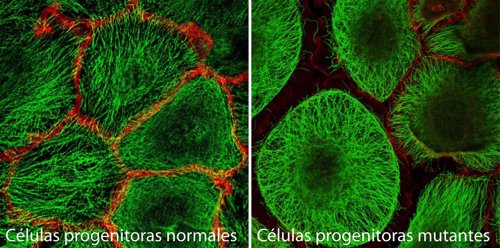
El primero consiste en identificar las células madre adultas de origen porcino, que sería el material biológico con propiedades terapéuticas. Por otro lado hay que desarrollar el patrón de osteoartritis o, lo que es lo mismo, originar la patología en los animales que van a servir como pacientes en la fase preclínica. «El reto innovador es provocar el daño siempre igual. Lo que estamos haciendo es buscar la mejor forma de generar la lesión en el cartílago», apunta Tapia, que añade que para hacerlo van a utilizar un equipo de ultrasonido y es que para que la investigación sea válida, la lesión tiene que ser la misma en todos los animales.
Una vez cumplimentadas estas dos fases, se trata de rellenar in vitro el biomaterial con las células madre para combinarlo todo. «Estas células poseen capacidades antiinflamatorias que reducirían la sintomatología pudiendo favorecer la regeneración osteoarticular», expone el director del proyecto.
El siguiente paso es implantar la combinación en el animal y realizar un seguimiento por técnicas de cirugía y de imagen, mediante resonancias magnéticas y artroscopias, para ver la evolución de las lesiones. «Esto durará entre tres y seis meses», adelanta García.
El final de la investigación consiste en tomar las muestras de las articulaciones de los animales en los que se haya implantado el biomaterial y, mediante técnicas de microscopía, determinar si el cartílago se ha recuperado correctamente de la lesión creada. «El cartílago es un tejido poco arraigado y de difícil regeneración, por lo que tendremos que ver si se mejora de la lesión y se recupera la funcionalidad de la articulación», afirma García.
El proyecto Cartman tiene como fecha de finalización el año 2015. «Hasta esa fecha nuestro objetivo será demostrar que el tratamiento es seguro y evaluar su efectividad», indica el investigador principal. En ese momento podría empezar lo que se denominaría como fase clínica, que supone que los hospitales pueden probar el biomaterial en pacientes humanos. «Una vez terminado nuestro proyecto, la Agencia del Medicamento tiene que aprobar su uso y, solo entonces, llegaría la fase clínica, que sería un proyecto nuevo», explica García, que define el tratamiento como paliativo y no preventivo y reconoce que este tipo de terapias siguen siendo aplicables en países ricos. Por lo que la idea del proyecto es la generación de biomateriales a bajo coste para que lleguen a la mayoría de los hospitales y a los países en vías de desarrollo.