Fuente:
http://www.elperiodico.com/es/noticias/salud-y-sanidad/hemos-regenerado-con-celulas-madre-hueso-cartilago-disco-vertebral-2622030
Dirige, junto con Robert Soler y en un centro médico privado, Teknon, la primera unidad de terapia celular de España que ha logrado regenerar hueso, disco vertebral y cartílago articular en personas que sufrían lesiones que no se soldaban tras una fractura o dolían por el desgaste. El equipo de Lluís Orozco (Tarragona, 1952) ha emprendido ahora la recomposición con altas dosis de células madre de cartílagos erosionados por la artrosis , un mundo sin fin (la artrosis afecta a más del 80% de los mayores de 65 años y a numerosos jóvenes deportistas) en el que, de momento, no tienen rival. Ni siquiera europeo, asegura. El objetivo médico y económico es de lo más atractivo.
EN LA CLÍNICA. El doctor Lluís Orozco, en su instituto, instalado en el Centro Médico Teknon de Barcelona.
-Se proponen solucionar con células madre la artrosis, una alteración que tarde o temprano afecta a casi todo el mundo, y muy dolorosa. Van a generar grandes expectativas.
-Lo sabemos. Y en eso estamos. La artrosis es la enfermedad más prevalente del aparato locomotor, en todas las razas y zonas geográficas. El 17% de la población española la sufre y la tiene diagnosticada. Y hay mucha gente joven que por un accidente o por lesiones tiene desgaste acelerado de las articulaciones.
-Ustedes frenan ese proceso, o lo revierten, utilizando células madre.
-Así es. Todos los tratamientos con células madre de la artrosis que hemos hecho, unos 140, han sido autorizados por la Agencia Española del Medicamento (las células madre son consideradas un fármaco por la legislación europea), y hemos publicado en la revista Trasplantation un ensayo clínico sobre 12 pacientes afectados por artrosis de rodilla.
-¿Con qué resultados?
-El 100% dejó de sentir dolor intenso a los pocos meses, y en 11 pacientes se observó una regeneración progresiva del cartílago. Objetivar que está habiendo una regeneración exige tiempo, es un proceso de más de un año. De momento, todos los tratados sienten gran alivio del dolor.
-Una larga incógnita.
-Sí. El cartílago es el tejido que más tarda en regenerarse. Pero hemos roto, o estamos rompiendo, un paradigma antiquísimo, del siglo XVII, que dice que el cartílago no se regenera porque es un tejido que no recibe sangre. Nosotros hemos provocado un nuevo fenómeno.
-¿Qué proceso han seguido?
- Con anestesia local y sedación ligera, aspiramos 100 mililitros de médula ósea de la pelvis de los pacientes futuros receptores. Esa médula es de fácil acceso y muy buena. Su aspecto se asemeja a la sangre, pero lleva adheridas unas pocas células madre, que están dormidas, no activas.
-Unas pocas.
Sí. Entonces las enviamos al laboratorio de cultivo, el Instituto de Biología Genética Molecular de Valladolid en el caso del ensayo clínico y el Banc de Sang i Teixits de Catalunya (BSTC) para el resto, donde se van seleccionando y captando. Un biorreactor las alimenta y multiplica, y produce una dosis de células puras.
-¿Cuántas copias?
-Para una artrosis, 40 millones de células. No se trata de un totum revolutum celular, sino de células puras, alimentadas con métodos de cultivo estandarizados y muy rigurosos.
-¿Y entonces?
-Nos las envían en una jeringuilla de 8 centímetros cúbicos. Las inyectamos en la articulación de la rodilla, y el paciente se va a su casa. Se le hace un seguimiento exhaustivo.
-¿Qué efecto provocan esas células?
-Crean cartílago, pero no son cartílago. Son células madre progenitoras, inmaduras. No son aún ningún tejido específico, pero colocadas en una articulación provocan que se activen los mecanismos biorregeneradores, y hacen cartílago. No sabemos si son ellas mismas o sus hijas. Sabemos que sobreviven y anidan.
-No saben del todo cómo sucede.
-El mecanismo íntimo de cómo se produce ese fenómeno no lo conocemos. Sabemos que cuando se inyectan en la rodilla unas mueren, pero otras sobreviven y anidan, generando unas sustancias regenerativas y antiinflamatorias con capacidad de crear sustancia cartilaginosa.
-¿Son antiinflamatorias?
-Lo son. Y como la artrosis es una enfermedad inflamatoria, matamos dos pájaros de un tiro: tratamos la inflamación y la regeneración del cartílago. Por eso lo primero que provocan es un gran alivio del dolor.
-¿Qué más notan los pacientes?
-En tres o cuatro meses, depende de la situación y edad de cada persona, perciben que desaparece la inflamación. Van mejorando la movilidad y se reduce la discapacidad. Más adelante, podremos objetivar la mejora del cartílago.
-¿Cómo miden la regeneración?
-Con un innovador sistema de medición por resonancia magnética. Tenemos 81 puntos de análisis de la rodilla, que son los que estudiamos para definir el patrón regenerativo. También puede aplicarse en tobillos, caderas, codos...
-¿En qué otros tejidos han aplicado la terapia celular?
-Hemos regenerado hueso, disco vertebral y cartílago articular. En el 2011, publicamos en Trasplantation otro ensayo con 10 pacientes que sufrían desgaste de disco vertebral. En cinco de ellos, la regeneración del disco se inició un año después de la inyección. También hemos tratado con células madre a pacientes que sufren falta de consolidación ósea. En total, hemos aplicado la terapia a 350 personas con patologías óseas.
-¿Falta de consolidación ósea?
-Huesos que no se sueldan tras una rotura, la cabeza del fémur, por ejemplo. En esos casos, hay varias cosas que hacer: estabilizar el hueso para que no se mueva, y aportarle proteínas u otras sustancias. Nosotros ofrecemos un injerto rico en células madre. Cuando digo rico, estoy diciendo muy rico: en dosis masivas. Dan buenos resultados, pero muy poco homogéneos a la hora de extraer conclusiones científicas.
-¿Cuándo iniciaron estas terapias?
-Empezamos con el BSTC en el 2002, con maquinaria de producción celular americana. En el 2004, la UE decretó que las células madre serían consideradas un medicamento. El instituto de Valladolid estaba preparado para esto y ese mismo año hicimos con ellos el primer estudio sobre disco vertebral y artrosis.
-¿Qué centros las aplican en España?
-Hay algo en la Clínica Universitaria de Navarra y en el Hospital Clínico Universitario de Salamanca. Durante muchos años, fuimos los únicos.
-¿Y en la sanidad pública?
-En el Hospital Vall d'Hebron están haciendo un ensayo sobre regeneración de huesos de cadera afectada por necrosis y discos lumbares, pero es muy reciente. Estamos diseñando un ensayo con el Servei Català de la Salut (CatSalut).
-¿Teknon y el CatSalut?
-Intentamos formar un equipo de investigadores en un hospital público (del que prefiero no dar el nombre) para aplicación de las células madre en el aparato locomotor. Será un estudio con gran número de pacientes. Si funciona, se introducirá en hospitales de excelencia como el Clínic o el Sant Pau, de Barcelona.
-Teknon es un centro privado.
-Un equipo privado que pertenece a la red de terapia celular del Estado, en el Instituto Carlos III, de Madrid, que es pública. Somos atípicos.
-¿Y caros?
-Un tratamiento de los nuestros cuesta unos 17.000 euros. Cultivo, transporte del material, aplicaciones, todo.
-¿Qué trayectoria de futuro prevé?
-Inmensa, la verdad. A día de hoy, ya hemos visto que tenemos una herramienta de una eficacia que nos ha sorprendido. Vamos en esa línea.
-¿En qué línea?
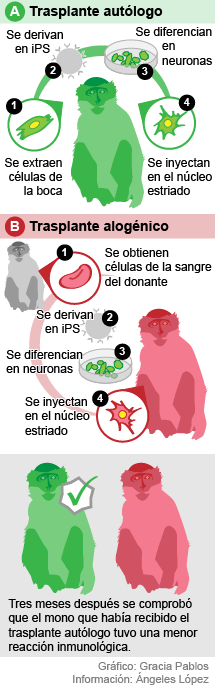
-Estamos haciendo estudios con células alogénicas: trasplante de un individuo a otro. Esto tiene interés para seropositivos del virus de la hepatitis o el sida. Las células madre alogénicas no generan rechazo, por lo que el paciente no necesitará tomar fármacos inmunosupresores.
-¿Cómo pudieron emprender un proyecto así en un centro privado?
-Teknon nos apoyó desde el minuto cero. Esta terapia tiene un gran potencial. Como las células madre se consideran un medicamento, es posible que la industria farmacéutica se interese por ellas. El problema lo tenemos con los saltimbanquis.
-¿Cómo dice?
-Sí. La palabra "célula" queda bien, y hay auténticas estafas. Utilizan la denominación de células madre sin serlo, porque el negocio a la vista es espectacular. Hablo a nivel internacional. Ofrecen dar vista a los ciegos y curar a los paralíticos. No aportan datos, pero hacen daño.